良好的组织固定是制备病理切片的前提,观察以下组织的切面,这些组织在固定时出现了什么问题?
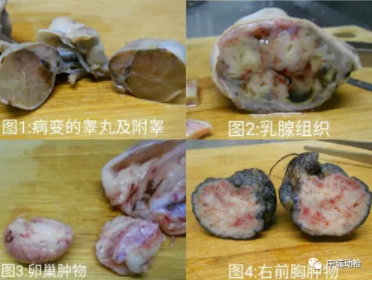
从图1-4的组织切面看,这4块组织在固定中出现了固定不充分的情况,颜色鲜艳,质地柔软,不易修块。需要进行二次固定才能进行切片,严重者组织中心发生自溶,无法进行病理学判读。
固定良好的样本颜色较暗,多为棕褐色,质地变硬,便于修块。如下图:

组织固定的目的是什么呢?
1. 为了能防止细菌腐蚀和组织的自溶,保持细胞原有的结构和形态。
2. 保存细胞固有物质,防止细胞内固有物质被破坏。
3. 使组织硬化,便于修块。
4. 有些标本可能具有传染性,及时固定可防止疾病扩散。
5. 标本经过及时彻底的固定后,可增强染色效果,利于诊断进行。
所以说组织固定是病理检测中及其重要的一步,固定的好坏,直接影响到切片的质量,进而影响组织病理的判读结果。
组织固定的细节你了解吗?
从组织学的角度,组织固定使组织尽量保持细胞、组织的固有形态和结构;而从免疫组化技术的角度,固定的作用不仅是使细胞内蛋白质凝固,尽量减少或终止外源性酶和内源性酶的反应,防止细胞自溶,以免使抗原扩散至组织间质,更重要的是保持组织或细胞的抗原性,不但要使抗原不失活,而且不使抗原发生弥散的现象,才能在免疫组化染色时,不产生过深的背景,影响对阳性物的判断。
组织固定需要注意什么?
1. 组织固定越新鲜越好。手术前准备好病理杯和固定液,组织一经离体,立刻放入固定。尤其是对某些酶的染色,固定最好在离体后的30s到1min 内。无特殊要求的最迟要求30min 内完成固定。
2. 组织块不宜过大过厚。组织厚度> 3cm,或者膜包裹的组织,进行分割后再固定,因为固定液的渗透是需要时间的,如果取材较厚,固定液还没有来得及到达组织深部,深部组织已经开始自溶了。
(自溶:组织离体后,不受机体管控,自身酶将组织分解而液化的过程。自溶的组织形态结构发生改变,无法进行组织病理学判读,故需严格执行组织固定注意事项和分割原则,避免自溶发生。)
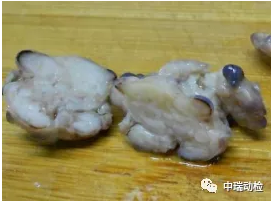
自溶组织,中心液化
组织分割原则:
1) 盛放组织的容器够大时,沿着组织的长轴或者短轴切成2cm 厚度,呈书页状,不用切断,保持一端连接,这样操作能够保持组织的原有形态和结构,便于取材。
2)组织有皮肤、鞘膜或其他生物膜包绕,将组织和膜沿一定方向切开,不用切断,保持一端连接,使固定液能够渗进组织;

切分示意图
3)组织过大,存放容器有限时,可以切成2cm*2cm*2cm 的块状,但组织边缘和与正常组织交界处,质地、颜色不同的组织交界处和眼观病变部位要带上。原始肿物进行拍照,并测量原肿物大小,将这些信息传递给送检实验室供病理老师参考。没有送实验室的剩余组织可以放置固定液中保存起来直到收到满意的病理报告后再处理掉。
3. 选择适当的固定液。目前使用的固定液浓度为4%的福尔马林,用38%-40%的甲醛原液,加入9倍体积的去离子水稀释而成。
4. 固定液量应为被固定标本体积的5~10倍。
5. 一般标本的固定时间为12~24小时,特殊组织或处理不当的组织须延长固定时间。
6. 提前配置或者购买合格的固定液,若紧急情况找不到固定液时,75%和95%酒精可以暂时代替福尔马林固定样本,需要注明酒精固定,并及时更换成福尔马林固定液。
组织固定是切片制作成功的第一步,临床医生不可忽视!